Ang Borane, anuman sa isang seryentong homologous ng mga organikong compound ng boron at hydrogen o ang kanilang mga derivatives.
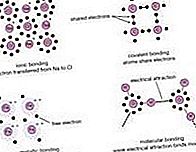
bonding ng kemikal: Mga boran
Ang compound na may kakulangan sa elektron, B2H6, tulad ng nabanggit kanina, ay maaaring ituring bilang isang kumpol ng mga atoms na gaganapin nang magkasama
Ang boron hydrides ay unang sistematikong synthesized at nailalarawan sa panahon ng 1912 hanggang humigit kumulang sa 1937 ng Aleman na chemist na si Alfred Stock. Tinawag niya ang mga ito ng mga boran sa pagkakatulad sa alkanes (saturated hydrocarbons), ang mga hydrides ng carbon (C), na siyang kapitbahay ng boron sa pana-panahong talahanayan. Dahil ang mas magaan na mga boran ay pabagu-bago ng isip, sensitibo sa hangin at kahalumigmigan, at nakakalason, ang Stock ay nakabuo ng mga pamamaraan ng high-vacuum at patakaran para sa pag-aaral sa kanila. Ang gawaing Amerikano sa mga boran ay nagsimula noong 1931, na isinagawa nina Hermann I. Schlesinger at Anton B. Burg. Ang mga boran ay nanatiling pangunahin ng interes sa akademiko hanggang sa Ikalawang Digmaang Pandaigdig, nang suportado ng gobyerno ng US ang paghahanap ng pabagu-bago ng mga compound ng uranium (borxidides) para sa paghihiwalay ng isotope, at noong 1950s, nang suportado ang mga programa upang makabuo ng mga high-fuel fuels para sa mga rocket at jet aircraft. (Ang mga boran at ang kanilang mga derivatives ay may mas mataas na pag-init ng pagkasunog kaysa sa mga gasolina ng hydrocarbon.) Si William Nunn Lipscomb, Jr., ay natanggap ang 1976 Nobel Prize for Chemistry "para sa kanyang pag-aaral sa istruktura ng mga boran na nagpapaliwanag ng mga problema ng bonding ng kemikal," habang ang isa sa Schlesinger's ang mga mag-aaral, si Herbert Charles Brown, ay nagbahagi ng 1979 na premyo para sa kanyang reaksyon ng haydroborasyon (1956), ang napakadaling pagdaragdag ng BH3 (sa anyo ng BH 3 · S) sa hindi nabubuong mga organikong compound (ibig sabihin, alkena at alkynes) sa eter solvents (S) sa temperatura ng silid upang magbunga ng mga organoboran na dami (iyon ay, sa isang reaksyon na magbubunga ng buo, o halos buo, hanggang sa pagkumpleto). Ang reaksyon ng haydroborasyon ay nagbukas ng mga bagong avenues ng pananaliksik sa lugar ng stereospecific organic synthesis.
Ang mga boran na inihanda ni Stock ay nagkaroon ng pangkalahatang komposisyon B n H n + 4 at B n H n + 6, ngunit ang mas kumplikadong mga species, parehong neutral at negatibo (anionic), ay kilala. Ang mga hydrides ng boron ay higit pa kaysa sa iba pang mga elemento maliban sa carbon. Ang pinakasimpleng ihiwalay na borane ay B 2 H 6, diborane (6). (Ang numeral na Arabe sa mga panaklong ay nagpapahiwatig ng bilang ng mga atomo ng hydrogen.) Ito ay isa sa mga pinaka-malawak na pinag-aralan at pinaka synthetically kapaki-pakinabang na mga intermediate na kemikal. Magagamit itong komersyal, at sa loob ng maraming taon maraming mga boran at ang kanilang mga derivatives ay inihanda mula dito, direkta man o hindi tuwiran. Ang libreng BH 3 (at B 3 H 7) ay hindi matatag, ngunit maaari silang ihiwalay bilang mga matatag na pagdaragdag (mga karagdagan na produkto) na may mga base ng Lewis (mga molekula ng elektron-donor) -eg, BH 3 · N (CH 3) 3. Ang mga boran ay maaaring solido, likido, o gas; sa pangkalahatan, ang kanilang mga natutunaw at kumukulo na mga puntos ay tumaas sa pagtaas ng pagiging kumplikado at molekular na timbang.
Istraktura at bonding ng mga boran
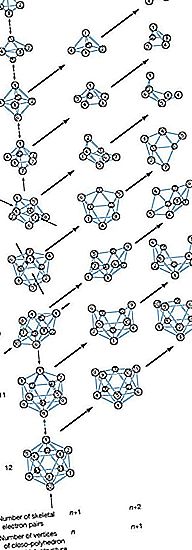
Sa halip na ipakita ang simpleng mga pagsasaayos ng chain at singsing ng mga compound ng carbon, ang mga atom ng boron sa mas kumplikadong mga boran ay matatagpuan sa mga sulok ng polyhedron, na maaaring isaalang-alang alinman sa mga deltahedron (polyhedron na may tatsulok na mukha) o mga fragment ng deltahedral. Ang pagbuo ng isang pag-unawa sa mga kumpol na boron na ito ay nagawa nang malaki upang matulungan ang mga chemists na mangangatwiran sa kimika ng iba pang mga tulagay, organometallic, at transition-metal na kumpol ng kumpol.
Ang isa sa ilang mga sistema ng nomenclature na iminungkahi ng International Union of Pure and Applied Chemistry (IUPAC) ay gumagamit ng mga katangian ng istruktura ng prefix: (1) closo- (isang katiwalian ng "clovo," mula sa Latin clovis, na nangangahulugang "hawla"), mga deltahedron ng n mga boron na atom; (2) nido- (mula sa Latin nidus, na nangangahulugang "pugad"), mga nonclosed na istruktura kung saan nasasakop ng B n cluster ang mga sulok ng isang (n + 1) -kulay na polyhedron — ibig sabihin, isang closo-polyhedron na may isang nawawalang vertex; (3) arachno- (Griyego, nangangahulugang "web spider"), mga kumpol na mas bukas, na may mga boron atoms na sumasakop sa mga magkadikit na sulok ng isang (n + 2) na may kulay na polyhedron — ibig sabihin, isang closo-polyhedron na may dalawang nawawalang vertice; (4) hypho- (Griyego, nangangahulugang "paghabi" o "isang lambat"), ang pinaka bukas na kumpol, na may mga boron na atom na sumasakop sa mga sulok ng isang (n + 3) -kutot na closo-polyhedron; at (5) klado- (Griyego, na nangangahulugang "sangay"), n mga patayo ng isang n + 4-vertex closo-polyhedron na inookupahan ng mga n boron atoms. Ang mga miyembro ng hypho- at klado-series ay kasalukuyang kilala lamang bilang mga derektibong borane. Ang ugnayan sa pagitan ng dalawa o higit pa sa mga kumpol na ito ng polyhedral borane ay ipinahiwatig ng prefix conjuncto- (Latin, na nangangahulugang "sumali ka"). Halimbawa, ang conjuncto-B 10 H 16 ay ginawa sa pamamagitan ng pagsali sa mga yunit ng B 3 H 8 mula sa dalawang B 6 H 9 na mga molekula sa pamamagitan ng isang b ― B bono.
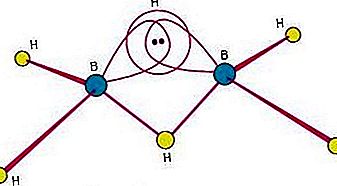
Ang isa sa mga dahilan ng malaking interes sa mga boran ay ang katotohanan na nagtataglay sila ng mga istruktura na naiiba sa anumang iba pang klase ng mga compound. Dahil ang bonding sa mga boran ay nagsasangkot ng multicentre bonding, kung saan ang tatlo o higit pang mga atom ay nagbabahagi ng isang pares ng mga bonding electrons, ang mga boran ay karaniwang tinatawag na mga sangkap na kulang sa elektron. Ang Diborane (6) ay may sumusunod na istraktura:
Ang istraktura na ito ay nagsasangkot ng three-center bridge bonding, kung saan ang isang pares ng elektron ay ibinahagi sa pagitan ng tatlo (sa halip na dalawa) na mga atom - dalawang boron na atom at isang hydrogen atom. (Tingnan ang bonding ng kemikal: Mga advanced na aspeto ng bonding ng kemikal: Mga banal na talakayan para sa talakayan ng three-center bond.) Ang kakayahan ng boron upang makabuo ng gayong mga bono bilang karagdagan sa normal na mga covalent bond ay humahantong sa pagbuo ng mga kumplikadong mga bordes ng polyhedral.