Ang prinsipyo ng pagbubukod ni Pauli, igiit na walang dalawang elektron sa isang atom ang maaaring maging sa parehong oras sa parehong estado o pagsasaayos, na iminungkahi (1925) ng Austrian na pisiko na si Wolfgang Pauli na account para sa mga sinusunod na pattern ng light emission mula sa mga atoms. Ang prinsipyo ng pagbubukod kasunod ay na-generalize upang isama ang isang buong klase ng mga particle na kung saan ang elektron ay isang miyembro lamang.
Ang mga subatomic particle ay nahuhulog sa dalawang klase, batay sa kanilang statistic na pag-uugali. Ang mga particle na kung saan nalalapat ang prinsipyo ng pagbubukod ng Pauli ay tinatawag na mga fermion; ang mga hindi sumusunod sa prinsipyong ito ay tinatawag na mga bosons. Kapag sa isang saradong sistema, tulad ng isang atom para sa mga electron o isang nucleus para sa mga proton at neutron, ang mga fermion ay ipinamamahagi upang ang isang naibigay na estado ay inookupahan lamang ng paisa-isa.
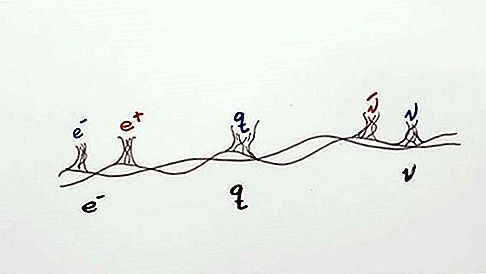
Ang mga partikulo na sumusunod sa prinsipyo ng pagbubukod ay may katangian na katangian ng pag-ikot, o intrinsic na angular momentum; ang kanilang pag-ikot ay palaging ilang mga kakatwa ng buong-bilang ng maraming isang-kalahati. Sa modernong pagtingin ng mga atomo, ang puwang na nakapalibot sa siksik na nucleus ay maaaring isipin na binubuo ng mga orbit, o mga rehiyon, na ang bawat isa ay binubuo lamang ng dalawang magkakaibang estado. Ang prinsipyo ng pagbubukod sa Pauli ay nagpapahiwatig na, kung ang isa sa mga estado na ito ay inookupahan ng isang elektron ng pag-ikot ng kalahati, ang iba ay maaaring sakupin lamang ng isang elektron ng kabaligtaran na pag-ikot, o iikot ang negatibong isang kalahati. Ang isang orbital na inookupahan ng isang pares ng mga electron na kabaligtaran na pag-ikot ay napuno: wala nang mga electron na maaaring pumasok dito hanggang sa isa sa mga pares ay nagbakasyon sa orbital. Ang isang alternatibong bersyon ng prinsipyo ng pagbubukod tulad ng inilalapat sa mga atomikong elektron ay nagsasaad na walang dalawang elektron ang maaaring magkaparehong mga halaga ng lahat ng apat na numero ng kabuuan.



![Ang gintong Rush film ni Chaplin [1925] Ang gintong Rush film ni Chaplin [1925]](https://images.thetopknowledge.com/img/entertainment-pop-culture/5/gold-rush-film-chaplin-1925.jpg)

![Aksidente sa Fukushima Japan [2011] Aksidente sa Fukushima Japan [2011]](https://images.thetopknowledge.com/img/technology/0/fukushima-accident-japan-2011.jpg)





