Ang Rhodium (Rh), elemento ng kemikal, isa sa mga metal na platinum ng Mga Grupo 8-10 (VIIIb), Mga Panahon 5 at 6, ng panaka-nakang talahanayan, na nakararami na ginagamit bilang isang alloying agent upang patigasin ang platinum. Ang Rhodium ay isang mahalagang, pilak-puting metal, na may mataas na pagmuni-muni para sa ilaw. Hindi ito corroded o tarnished ng kapaligiran sa temperatura ng silid at madalas na electroplated sa mga bagay na metal at pinakintab upang magbigay ng permanenteng, kaakit-akit na ibabaw para sa alahas at iba pang mga pampalamuti na artikulo. Ginagamit din ang metal upang makabuo ng mga sumasalamin na ibabaw para sa mga optical na instrumento.
Ang Rhodium ay idinagdag sa platinum sa maliit na halaga ay nagbubunga ng mga haluang metal na mas mahirap at mawalan ng timbang sa mataas na temperatura kahit na mas mabagal kaysa sa purong platinum. Ang ganitong mga haluang metal ay ginagamit para sa mga crucibles ng pugon sa laboratoryo, mga spark-plug electrodes, at mga katalista sa sobrang init na mga kemikal na kapaligiran (kabilang ang mga automobile na catalytic convert). Sa paggawa ng pang-industriya na nitric acid, ang mga gauze catalysts ng rhodium-platinum na haluang metal ay ginagamit dahil maaari nilang mapaglabanan ang temperatura ng siga habang ang ammonia ay sinunog sa nitric oxide. Ang isang wire ng haluang metal 10 porsyento na rhodium-90 porsyento na platinum ay sumali sa isang kawad ng purong platinum na bumubuo ng isang mahusay na thermocouple para sa pagsukat ng mataas na temperatura sa isang naka-oxidizing na kapaligiran. Ang internasyonal na scale ng temperatura ay tinukoy sa rehiyon mula sa 660 ° hanggang 1,063 ° C (1,220 ° hanggang 1,945 ° F) sa pamamagitan ng elektromotiko na puwersa ng thermocouple na ito.
Ang Rhodium ay isang bihirang elemento na binubuo ng hanggang sa 4.6 porsyento ng mga katutubong platinum na haluang metal. Nagaganap din ito sa mga katutubong haluang metal ng iridium at osmium: hanggang sa hindi bababa sa 11.25 porsyento sa iridosmine at hanggang sa hindi bababa sa 4.5 porsyento sa siserskite. Ang Rhodium ay nangyayari sa likas na katangian na may kaugnayan sa iba pang mga metal na metal na platinum, at ang paghihiwalay at pagpipino nito ay bahagi ng pangkalahatang pagproseso ng metalurhiko ng grupo. Ang Rhodium sa pangkalahatan ay nakuha sa komersyo bilang isang produkto ng pagkuha ng nikel at tanso mula sa kanilang mga ores.
Ang natural na rhodium ay binubuo nang buo ng matatag na isotopang rhodium-103. Ang elemento ay una na nakahiwalay (1803) mula sa crude platinum ng botika ng Ingles at pisisista na si William Hyde Wollaston, na pinangalanan ito mula sa Greek rhodon ("rose") para sa pulang kulay ng isang bilang ng mga compound nito. Ang Rhodium ay lubos na lumalaban sa pag-atake ng mga acid; ang napakalaking metal ay hindi natutunaw ng mainit na puro nitrik o hydrochloric acid o kahit sa pamamagitan ng aqua regia. Ang metal ay natunaw sa fused potassium hydrogen sulfate upang magbunga ng isang kumplikado, natutunaw na tubig na sulfate K 3 Rh (SO 4) 3 · 12H 2 O, sa mainit na puro sulpuriko acid, at sa puro hydrochloric acid na naglalaman ng sodium perchlorate sa 125 ° –150 ° C (257 ° –302 ° F).
Ang sentro ng kimika ng Rhodium higit sa lahat sa mga estado ng +1 at +3; ang ilang mga compound ng iba pang positibong estado ng oksihenasyon sa pamamagitan ng +6 ay kinikilala. Ang Rhodium ay bumubuo ng dirhodium tetraacetate, Rh 2 (O 2 CCH 3) 4 at iba't ibang mga derivatibo na naglalaman ng dalawang karagdagang laso - halimbawa, tubig, pyridine, o triphenylphosphine - sa estado ng oksihenasyon +2. Ang mga kumplikado sa estado ng oksihenasyon +1 pangunahin ay naglalaman ng carbon monoxide, olefins, at mga phosphine bilang mga ligand. Ang lahat ng mga compound ng rhodium ay madaling mabawasan o mabulok sa pamamagitan ng pag-init upang magbunga ng pulbos o espongha na metal. Kabilang sa mga compound na rhodium trichloride na ito, ang RhCl 3 (kung saan ang rhodium ay nasa +3 na estado), ay isa sa pinakamahalaga. Nagbibigay ito ng isang panimulang materyal para sa marami sa iba pang mga rhodium compound sa iba't ibang mga estado ng oksihenasyon. Sa isang may tubig na emulsyon maaari itong paganahin ang isang bilang ng mga kapaki-pakinabang na organikong reaksyon.
Mga Katangian ng Elemento
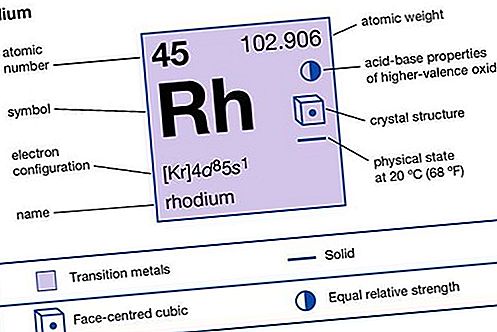
| numero ng atomic | 45 |
|---|---|
| konting bigat | 102.905 |
| temperatura ng pagkatunaw | 1,966 ° C (3,571 ° F) |
| punto ng pag-kulo | 3,727 ° C (6,741 ° F) |
| tiyak na gravity | 12.4 (20 ° C) |
| estado ng oksihenasyon | +1, +2, +3, +4, +5, +6 |
| config ng electron. | [Kr] 4d 8 5s 1 |







![Pagsalakay sa pelikulang Body Snatcher ni Siegel [1956] Pagsalakay sa pelikulang Body Snatcher ni Siegel [1956]](https://images.thetopknowledge.com/img/entertainment-pop-culture/2/invasion-body-snatchers-film-siegel-1956.jpg)



![Quebec Act Great Britain [1774] Quebec Act Great Britain [1774]](https://images.thetopknowledge.com/img/politics-law-government/5/quebec-act-great-britain-1774.jpg)

