Sulfide, na-spell din sulphide, alinman sa tatlong mga klase ng mga kemikal na compound na naglalaman ng elemento ng asupre. Ang tatlong klase ng mga sulfide ay may kasamang mga organikong sulfide, organikong sulfide (kung minsan ay tinatawag na thioethers), at posporus na mga sulfide. Ang mga organikong sulfide ay mga ionic compound na naglalaman ng negatibong sisingilin na sulfide ion, S 2−; ang mga compound na ito ay maaaring ituring bilang mga asing-gamot sa sobrang mahina acid hydrogen sulfide. Ang mga organikong sulfide ay mga compound kung saan ang isang asupre na asupre ay covalently bonded sa dalawang mga organikong grupo. Ang Phosphine sulfides ay nabuo mula sa reaksyon ng mga organikong phosphine na may asupre, kung saan ang atom ng asupre ay nauugnay sa posporus sa pamamagitan ng isang bono na may parehong mga katangian ng covalent at ionic.

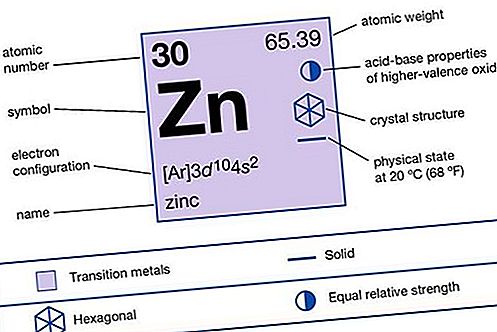
Ang mga suliranin ng maraming mahalagang elemento ng metal ay natural na nagaganap na mga mineral. Halimbawa, ang pyrite, na tinatawag ding gintong tanga dahil sa brassy dilaw na kulay nito, ay isang sulfide na bakal na may formula FeS 2. Ang Pyrite ay isang pangunahing mapagkukunan ng bakal at isa sa pinaka-sagana ng mineral na asupre. Ang zinc, cadmium, mercury, tanso, pilak, at maraming iba pang mga elemento ay nangyayari sa kalikasan bilang mga sulfide.
Paghahanda ng mga sulfide
Karamihan sa mga metal ay direktang tumugon sa asupre upang mabuo ang mga metal na sulfide - ibig sabihin, mga compound na naglalaman ng isang metal na atom at ang sulfide ion, S 2−. Bilang karagdagan sa direktang pagsasama ng mga elemento bilang isang paraan ng paghahanda ng mga sulfide, maaari rin silang magawa sa pamamagitan ng pagbawas ng isang sulpate sa pamamagitan ng carbon o sa pamamagitan ng pag-ulan mula sa acidic aqueous solution sa pamamagitan ng hydrogen sulfide, H 2 S, o mula sa pangunahing solusyon sa pamamagitan ng ammonium sulfide, (NH 4) 2 S. Ang isa pang pamamaraan, lalo na angkop para sa mga natutunaw na tubig na sulfide, ay nagsasangkot ng pagbulwak H 2 S sa isang pangunahing solusyon ng metal upang mabigyan ang metal hydrogen sulfide, MHS. Ang isang karagdagang katumbas ng idinagdag na metal hydroxide ay magbubunga ng metal sulfide. NaOH + H 2 S → NaHS + H 2 O
NaHS + NaOH → Na 2 S + H 2 O
Solubility ng sulfides
Ang mga metal na alkali at mga alkalina na metal na metal ay ang tanging mga sulfide na may anumang naaapektuhan na solubility ng tubig at lumilitaw na pangunahing ionik. Sa kaibahan, ang mga sulfide ng tanso ng tanso at zinc ay ilan sa mga hindi bababa sa nalulusaw na mga compound na kilala. Kapag ang tubig na natutunaw ng tubig na metal ay pinainit sa may tubig na solusyon na may elemento ng asupre, nabuo ang mga solusyon ng tinatawag na polysulfides. Ang mga solusyon na ito ay pangunahing binubuo ng S 4 2− at S 3 2− anion. Ang mga sulfide ay isang mahalagang sangkap ng mga mapagkukunan ng kapangyarihan na may mataas na density tulad ng lithium at baterya ng sodium sulfide. Ang mga sulfide na ginamit sa mga mapagkukunang kapangyarihan na ito ay M 2 S, M 2 S 2, M 2 S 4, at M 2 S 5.