Scandium (Sc), elemento ng kemikal, isang bihirang-lupa metal ng Pangkat 3 ng pana-panahong talahanayan.
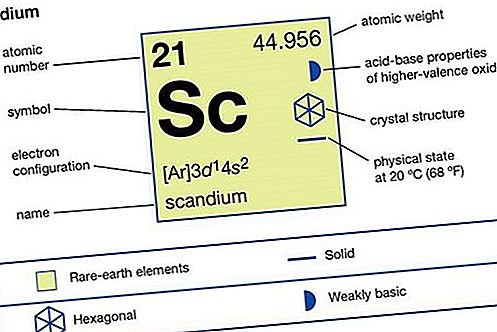
Ang Scandium ay isang kulay-pilak na puting, katamtaman na malambot na metal. Ito ay medyo matatag sa hangin ngunit dahan-dahang baguhin ang kulay nito mula sa pilak na puti hanggang sa isang madilaw-dilaw na hitsura dahil sa pagbuo ng Sc 2 O 3 oxide sa ibabaw. Ang metal ay dahan-dahang natutunaw sa diluted acid - maliban sa hydrofluoric acid (HF), kung saan pinipigilan ang isang proteksiyon na layer ng trifluoride. Ang Scandium ay paramagnetic mula sa 0 K (−273 ° C, o −460 ° F) hanggang sa pagtunaw nito (1,541 ° C, o 2,806 ° F). Ito ay nagiging superconducting sa −273.1 ° C (−459.6 ° F) sa mga presyon na lumampas sa 186 kilobars.
Matapos ang chemist ng Ruso na si Dmitry Ivanovich Mendeleyev noong 1871 ay hinulaan ang pagkakaroon ng sangkap na ito, pansamantalang tinawag itong ekaboron, ang chemist ng Sweden na si Lars Fredrik Nilson noong 1879 ay natuklasan ang oxide, scandia, sa bihirang-lupa na gadolinite at euxenite, at chemist ng Suweko na Per Teodor Cleve sa bandang huli noong 1879 nakilala ang scandium bilang hypothetical ekaboron. Ang Scandium ay matatagpuan sa maliit na proporsyon, sa pangkalahatan mas mababa sa 0.2 porsyento, sa marami sa mga mabibigat na lanthanide ores at sa maraming mga lata, uranium, at tungsten ores. Ang Thortveitite (isang scandium silicate) ay ang tanging mineral na naglalaman ng malaking halaga ng scandium, halos 34 porsyento, ngunit sa kasamaang palad, ang mineral na ito ay medyo bihirang at hindi isang mahalagang mapagkukunan ng scandium. Ang kosmic kasaganaan ng scandium ay medyo mataas. Kahit na ito ay tungkol lamang sa ika-50 pinaka-masaganang elemento sa Earth (ang kasaganaan nito ay katulad ng beryllium), ito ay tungkol sa ika-23 pinaka-masaganang elemento sa Araw.
Sa likas na katangian, ang scandium ay umiiral sa anyo ng isang matatag na isotop, scandium-45. Kabilang sa 25 (hindi kasama ang mga isomer ng nuklear) na isotopikong radioactive na may masa na nagmula sa 36 hanggang 61, ang pinaka-matatag ay scandium-46 (kalahating buhay ng 83.79 na araw), at ang hindi bababa sa matatag ay scandium-39 (kalahating buhay ng mas mababa sa 300 nanoseconds).
Ang Scandium ay nahihiwalay mula sa iba pang mga bihirang mga lupa sa pamamagitan ng pag-ulan ng hindi matutunaw na potasa scandium sulfate o sa pamamagitan ng pagkuha ng scandium thiocyanate ng diethyl eter. Ang metal mismo ay unang inihanda noong 1938 ng electrolysis ng potasa, lithium, at scandium chlorides sa isang eutectic halo (ibig sabihin, isang halo na may pinakamababang punto ng pagtunaw na posible sa mga sangkap). Ang Scandium ngayon ay ginawa ng karamihan bilang isang by-product ng uranium extraction mula sa mineral davidite, na naglalaman ng halos 0,02 porsyento na scandium oxide. Ang Scandium ay umiiral sa dalawang pormasyong allotropic (istruktura). Ang α-phase ay malapit na puno ng heksagonal na may isang = 3.3088 Å at c = 5.2680 Å sa temperatura ng silid. Ang β-phase ay body-centic cubic na may tinatayang isang = 3.73 Å sa 1,337 ° C (2,439 ° F).
Ilan lamang ang paggamit ng hindi pangkaraniwang paglipat ng metal na ito na binuo, na karamihan ay dahil sa limitadong pagkakaroon ng scandium at mataas na gastos. Ang mababang density nito at mataas na punto ng pagkatunaw ay nagmumungkahi ng mga application bilang isang ahente ng alloying para sa magaan na metal para sa mga aplikasyon ng militar at mataas na pagganap. Ang mga pangunahing paggamit ng scandium ay bilang isang addoy ng haluang metal sa alloy na nakabase sa aluminyo para sa mga gamit sa palakasan at sa mga lampara na metal halide na may mataas na lakas. Kapag pinagsama ng alloy at aluminyo na batay sa aluminyo, nililimitahan ng scandium ang paglago ng butil na may mataas na temperatura.
Ang kimika ng scandium ay mas malapit na pagkakahawig ng iba pang mga bihirang-lupa na elemento ng oksihenasyon ng estado +3 kaysa sa aluminyo o titan. Ang ilan sa pag-uugali nito, gayunpaman, ay atypical sa mga bihirang mga lupa dahil sa makabuluhang mas maliit na ionic radius (1.66 Å para sa koordinasyon bilang 12) kung ihahambing sa bihirang-lupa average (1.82 Å para sa koordinasyon na numero 12). Para sa kadahilanang ito, ang Sc 3+ ion ay isang medyo malakas na acid at may higit na higit na pagkahilig upang makabuo ng mga kumplikadong ions.
Mga Katangian ng Elemento
| numero ng atomic | 21 |
|---|---|
| konting bigat | 44.95591 |
| temperatura ng pagkatunaw | 1,541 ° C (2,806 ° F) |
| punto ng pag-kulo | 2,836 ° C (5,137 ° F) |
| tiyak na gravity | 2.989 (24 ° C, o 75 ° F) |
| estado ng oksihenasyon | +3 |
| pagsasaayos ng elektron | [Ar] 3d 1 4s 2 |









![Labanan ng Plassey kasaysayan ng India [1757] Labanan ng Plassey kasaysayan ng India [1757]](https://images.thetopknowledge.com/img/world-history/5/battle-plassey-indian-history-1757.jpg)


